初中氧化反应和氧化还原反应的区别
一、性质不同
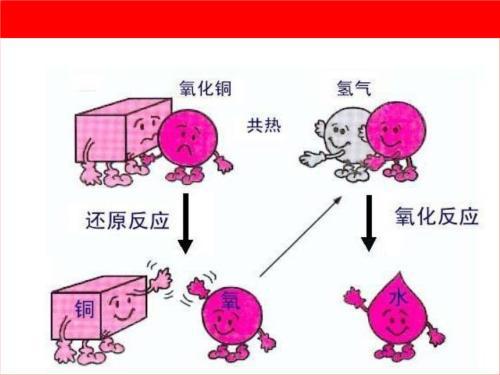
1、氧化反应:是物质与氧发生的化学反应,氧气在此过程中提供氧。
2、氧化还原反应:是化学反应前后,元素的氧化数有变化的一类反应。
二、特点不同
1、氧化反应:。氧化时氧化值升高;还原时氧化值降低。氧化、还原都指反应物(分子、离子或原子)。
2、氧化还原反应:电子的得失或共用电子对的偏移。
扩展资料:
氧化还原反应中,存在以下一般规律:
1、强弱律:氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物。
2、价态律:元素处于最高价态,只具有氧化性;元素处于最低价态,只具有还原性;处于中间价态,既具氧化性,又具有还原性。
3、转化律:同种元素不同价态间发生归中反应时,元素的氧化数只接近而不交叉,最多达到同种价态 。
4、优先律:对于同一氧化剂,当存在多种还原剂时,通常先和还原性最强的还原剂反应。
5、守恒律:氧化剂得到电子的数目等于还原剂失去电子的数目。
参考资料来源:搜狗百科-氧化反应
参考资料来源:搜狗百科-氧化还原反应
标签:氧化,反应,初中
版权声明:文章由 酷百书 整理收集,来源于互联网或者用户投稿,如有侵权,请联系我们,我们会立即处理。如转载请保留本文链接:https://www.kubaishu.com/article/121172.html