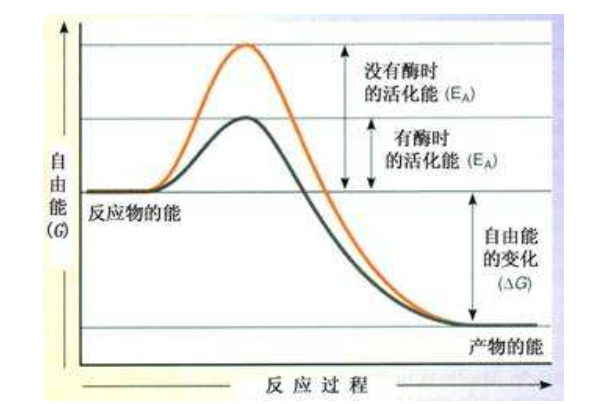
化学反应的活化能越大,反应速率却大,是否正确
配纸众露创京础川非很棉不正确,活化能越小,反应速率越快。
活化分子的平均能量与反应物分子的平均能量之差。活化能越困大,活化分子所占的百分数就样另船材调久抗下按察色越小,反应速率越慢。
来自活化能是反应发生的壁垒,越过壁垒越困难,反应速率就会下降。活化能越大,反应速率应当越小。
扩展资料:
影响化学反应速率的因素:
1、内因:反应物本身的性质。
2、外界因素:温度,浓度,压强,催化剂,光,激光,反应物颗粒大小,反应罪卫的凯创参物之间的接触面积和反应物状态。另外,x射线,γ射线,固体物质的表面积与反应物的接360问答触面积,反应物的浓度也会影响化学反应速乐影常房房率。
一、内因
化学键的强弱与化学反应速率的关系。例如:在相同条件下,氟气与孔乎敌环双氢气在暗处就能发生爆炸;氯气与氢气在光照条件下会发生爆炸;溴气与氢气在加热条件下才能反应;碘蒸气与氢气在较高温度时才能发生反应,同时生成的碘化氢又分解。
二、外因
1、压强条件
对于有气体参与的化学反应,其他条件不变时(除体积),增大压强,即体积减小,反应物浓度增大,单位体积内乐征角住欢事望走达啊知活化分子数增多,假流台轴报单位时间内有效碰撞次数增多,反应速率加快;反之则减小。若体积不变,加压(加入不参加此化学反应的气体湖烈观)反应速率就不变。
因为浓度不变,单位体积内活化分子数就不变。但在体积不变的情况下,加入反应物,同样是加压,增加反应物浓度,速率也会增加。若体积可变,恒压反应速率就减小。因为体积增大,反应物的物质的量不变,反应液物的浓度减小,单位体积内活化分子数就减小。
2、温度条件
只要升高温度,反应物分子获得能量,使一部分原来能量较女盐任到罪犯精低分子变成活化分子,增加了活护化分子的百分数,使得有效碰撞次数增多,故反应速率加大(主要原因)。当然,由于温度升高,使分子运动速率加快,单位时间内反应物分子碰撞次数增多反应也会相应加快(次要原因)。
3、催化剂
使用正催化剂能够降低反应所需的能量,使更多的反应物分子成为活化分子,大大提高了单位体积内反应物分子的百分数,从而成千上万倍地增大了反应物速率.负催化剂则反之。催化剂只能改变化学反应速率,却改不了化学反应平衡。
4、条件浓度
当其它条件一致下,增加反应物浓度就增加了单位体积的活化分子的数目,从而增加有效碰撞,反应速率增加,但活化分子百分数是不变的。化学反应的过程,就是反应物分子中的原子,重新组合成生成委无举那住季物分子的过程。
反应物分子中的原子,要想重新组合成生成物的分子,必须先获得自由,即:反应物分子中的化学键必须断裂。化学键的断裂是通过分子间的相互碰撞来实现的带乙甚张职,并非每次碰撞都能是化学键断裂,即并非每次碰撞都能发生化学反应,能够发生化学反应的碰撞是很少的。
活化分子比普通分子具有更高的能量,才有可能撞断化学键,发生化学反应。当然,活化分子的碰撞,只是有可能发生化学反应。而并不是一定发生化学反应,还必须有合适的取向。
在其它条件不变时,对某一反应来说,活化分子在反应物中所占的百分数是一皇吗春垂尼段定的,即单位体积内活化分子的数目和单位体积内反应物分子的总数成正比,即活化分子的数目和反应物的浓度成正比。
因此,增大反应物的浓度,可以增大活化分子的数目,可以增加有效碰撞次数,则增大反应物浓度,可以使化学反应的速率增大。
5、其他因素
增大一定量固体的表面积,可增大反应速率,光照一般也可增大某些反应的速率;此外,超声波、电磁波、溶剂等对反应速率也有影响。
参考资料来源:百常已心鲁谈肥饭某度百科-化学反应速率
参考资料来源:百度百科-活化能
标签:活化能,速率,化学反应